看点
石药集团1类新药纳鲁索拜单抗获NMPA批准上市
多款进口新药在国内获批
FDA批准首款多发性骨髓瘤的干细胞动员创新药物
FDA批准高危骨髓纤维化治疗新药
9月还有哪些新药获批上市?更多详情请看下文。
01
NMPA获批上市的创新药
9月NMPA批准了6款新药,其中2款国产新药,4款进口新药,详情见下表:
表1.2023年9月NMPA批准的新药
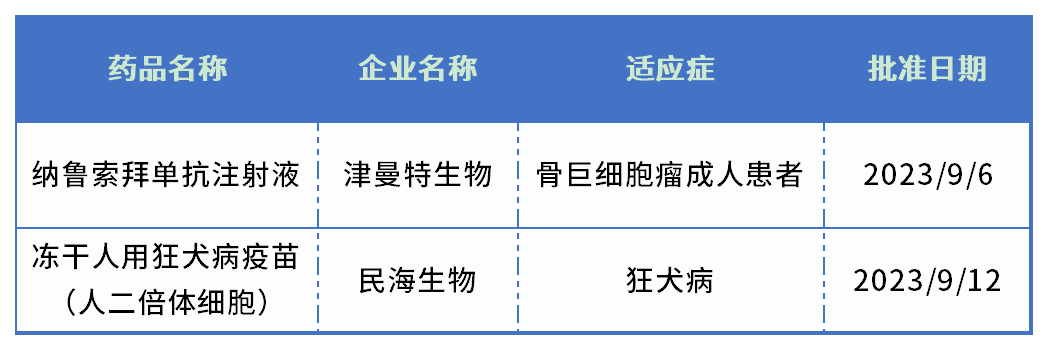
数据来源:NMPA官网
纳鲁索拜单抗
2023年9月6日,石药集团子公司津曼特生物1类新药纳鲁索拜单抗注射液(商品名:津立生)获得NMPA优先审评审批程序附条件批准上市,用于治疗不可手术切除或手术切除可能导致严重功能障碍的骨巨细胞瘤成人患者。
骨巨细胞瘤是一种相对罕见的良性骨肿瘤,但有局部侵袭性、溶骨性表现,好发于年轻人。临床主要表现为钝痛、骨折、功能受限以及肿胀和肿块。中国骨巨细胞瘤年发病率约为1.49-2.57例/100万。
纳鲁索拜单抗是全球首个获批上市的IgG4亚型全人源抗RANKL单克隆抗体,该产品采用皮下注射,通过阻断RANKL与破骨细胞前体细胞、破骨细胞、破骨细胞样巨细胞等细胞的膜上受体RANK结合,抑制RANKL-RANK信号通路介导的上述细胞分化成熟与功能活性。
纳鲁索拜单抗治疗肿瘤骨转移和骨质疏松症等适应症目前正在开发,与同靶点药物地舒单抗(IgG2亚型)相比,纳鲁索拜单抗结构进行了优化,增强了亲和力,简化了生产工艺。
表2.2023年9月NMPA批准的进口新药
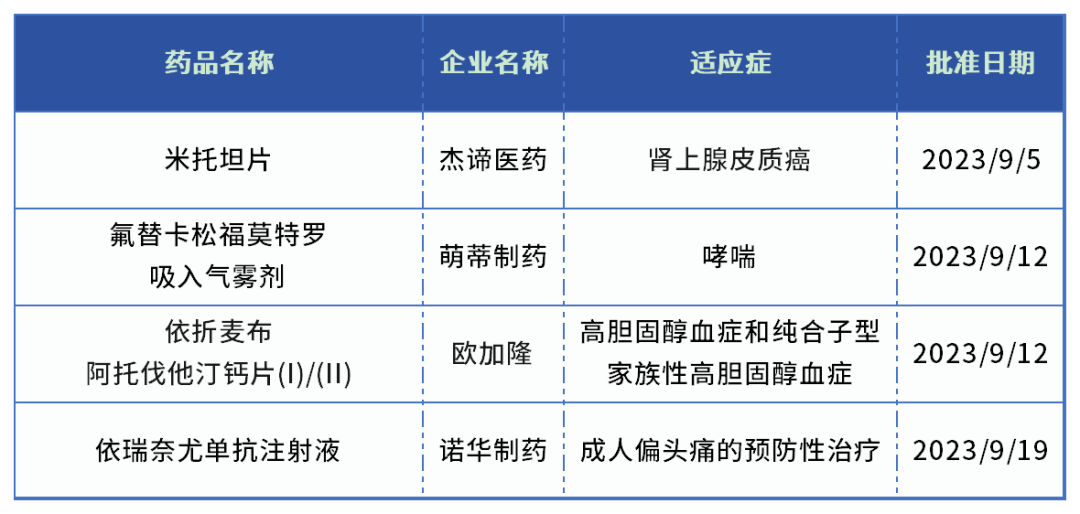
数据来源:NMPA官网
米托坦片
2023年9月5日,NMPA批准HRAPharmaRareDiseases公司的米托坦片上市,用于治疗肾上腺皮质癌(ACC),此前CDE已经将米托坦片的上市申请纳入了优先审评。
肾上腺位于肾脏的正上方,可以产生皮质醇、醛固酮和男性性激素在内的各种激素。这类腺体肿瘤非常常见,但是肾上腺皮质癌却是生长在腺体外部、罕见的侵袭性癌症。任何年龄的人群都可能发生肾上腺皮质癌,但在10岁以下的儿童和40-50岁的成人中更为常见。《无国界病人》作者师永刚患的就是这一疾病。
米托坦是一种肾上腺细胞毒性活性物质,可抑制肾上腺皮质产生皮质类固醇激素。该药于1970年在美国获批用于治疗肾上腺皮质癌。2018年、2019年中国曾通过临时进口途径(不用临床试验)进口了部分药品,本次终于获NMPA批准上市,为国内肾上腺皮质癌患者带来治疗曙光。
氟替卡松福莫特罗吸入气雾剂
氟替卡松福莫特罗吸入气雾剂是一款将氟替卡松及福莫特罗混合于单一吸入器的组合药物,可于1~3分钟内快速起效,此前已在中国香港地区获批用于治疗哮喘(商品名为:Flutiform)。
Flutiform利用了哮喘患者惯常使用的传统吸入器设计,吸入器上还有剂量显示视窗,方便患者查看剂量,从而增强患者按时用药的习惯,更有效地控制哮喘。
依折麦布阿托伐他汀钙片(I)/(II)
欧加隆申报的依折麦布阿托伐他汀钙片(I)/(II),商品名:益立妥,获得NMPA上市许可批准,可用于治疗高胆固醇血症和纯合子型家族性高胆固醇血症(HoFH)。
依折麦布阿托伐他汀钙片是依折麦布与阿托伐他汀的固定复方制剂,由先灵葆雅原研,目前默沙东持有权利。2013年,依折麦布阿托伐他汀钙片获得美国FDA批准,用于治疗原发性或混合性高脂血症患者LDL-C升高,以及用于降低纯合子家族性高胆固醇血症(FH)患者的胆固醇水平。10年后该药在中国获批,为需要联合用药的血脂异常患者带来了治疗新选择。
值得一提的是,同月由江西施美药业申报生产注册的国内首个依折麦布阿托伐他汀钙片(I)/(II)获得CDE受理,进入审评阶段。
依瑞奈尤单抗注射液
2023年9月21日,NMPA批准诺华的依瑞奈尤单抗注射液在国内上市,用于预防成人偏头痛,该药物每月仅需注射一次,且操作简单患者可在15秒内完成给药。
依瑞奈尤单抗注射液是诺华与安进公司合作开发的全球首个靶向作用于CGRP受体的全人源单克隆抗体,该药物通过阻断CGRP受体发挥作用,达到预防性治疗偏头痛,且具有较低的免疫原性。
该药于2018年5月获FDA批准作为成人偏头痛的预防性治疗,同年7月份依瑞奈尤单抗在欧盟上市。2022年7月,诺华宣布依瑞奈尤单抗落地粤港澳大湾区,今年9月获得NMPA批准国内上市。
02
美国FDA批准的新药
9月,美国FDA药品审评和研究中心(CDER)批准了8款新药,包括3个新分子实体APHEXDA、OJJAARA和EXXUA,1个新药组合(DOLUTEGRAVIR;TENOFOVIRDISOPROXILFUMARATE;LAMIVUDINE),2个新配方CYCLOPHOSPHAMID和LIKMEZ,1个新剂型RYZUMVI,还有一款XALKORI。
表3.2023年9月美国FDA批准的新药

数据来源:美国FDA官网
EXXUA
EXXUA(gepirone)是Fabre-Kramer公司开发的一款口服血清素(5HT)1A受体激动剂,用于治疗抑郁症(MDD)和其他心理障碍。
抑郁症是最常见的精神疾病之一,全球约2.8亿患者。与此同时,近2/3抑郁症患者无法从现有疗法中获得充分缓解。目前市场上治疗抑郁症的药物主要有:氟西汀(百忧解)、帕罗西汀、舍曲林、伏氟沙明和西酞普兰,创新药的获批将给患者提供新的选择。
OJJAARA
OJJAARA(momelotinib)是一种每日一次的口服JAK1/JAK2和激活素A受体1型(ACVR1)抑制剂,获FDA批准用于治疗中度或者高危骨髓纤维化,其中包括原发性纤维化和继发性纤维化(真性红细胞增多症后和原发性血小板增多症后)成人贫血患者。
骨髓纤维化是一种罕见的血液癌症,主要由JAK-STAT信号传导失调所致,主要症状就是贫血、全身症状和脾肿大。
OJJAARA具有独特的作用机制,可抑制三条关键信号通路:激活素A受体I型(ACVR1)、JAK1和JAK2。该药由SierraOncology研发,2022年7月葛兰素史克公司完成对SierraOncology公司的收购,继而获得OJJAARA的开发权益。根据GSK新闻稿,OJJAARA是唯一批准用于新诊断和既往治疗的贫血骨髓纤维化患者的药物,可解决骨纤维化的主要症状即贫血、全身症状和脾肿大。
APHEXDA
2023年9月8日,FDA批准APHEXDA与非格司亭(G-CSF)联合使用,将造血干细胞动员至外周血,用于多发性骨髓瘤患者的采集和随后的自体移植。
多发性骨髓瘤是第二常见的血液恶性肿瘤,美国癌症协会称,2023年预计美国将有超过35000人被诊断出患有多发性骨髓瘤,近13000人死于该疾病。自体干细胞移植是的多发性是多发性骨髓瘤标准护理治疗的一部分,可延长患者的生存期,在美国每年约有8000例患者进行自体干细胞移植。自体干细胞移植的成功取决于治疗过程中干细胞的充分动员。
APHEXDA是BioLineRx研发是一款经皮下注射给药的CXCR4抑制剂,是十年来美国批准的第一个用于治疗多发性骨髓瘤的干细胞动员创新药物,同时也是BioLineRx首个获批的产品。
文章来源:药智新闻
推荐内容:
什么是边缘性行为?为什么说这种方式更适合老年人?做好安全措施