近日,康宁杰瑞与石药集团共同宣布,HER2双特异性抗体注射液(研发代号:KN026)联合注射用多西他赛(白蛋白结合型)用于一线治疗HER2阳性复发转移性乳腺癌的注册临床试验申请在中国获批。
该研究是一项随机、对照、开放、多中心Ⅲ期临床研究,计划入组880例受试者,旨在评估KN026联合多西他赛白蛋白结合型对比曲妥珠单抗联合帕妥珠单抗和多西他赛一线治疗HER2阳性转移性乳腺癌患者的有效性和安全性。主要研究终点为经独立评审委员会(IRC)评估的无进展生存期(PFS)。
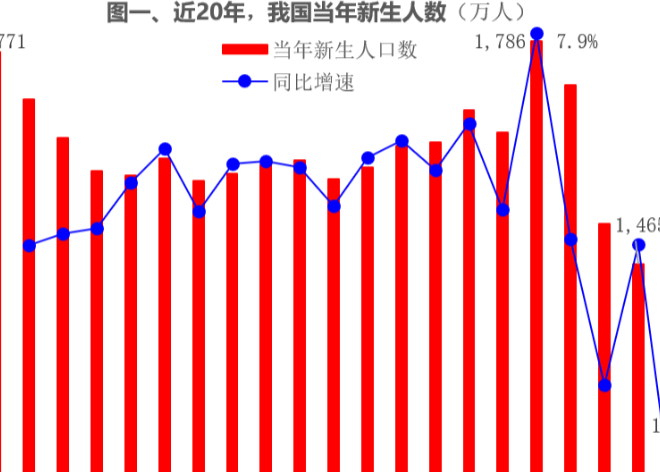
乳腺癌是全球女性最常见的恶性肿瘤,世界卫生组织报告显示,平均每1.8秒就有1例乳腺癌患者确诊。而在中国,乳腺癌患病率逐年增高,2020年新增数量高达42万例,并导致12万例患者死亡。随着科学技术的进步,早期乳腺癌患者的生存得到了显著改善,但HER2阳性乳腺癌侵袭性强、异质性高、易复发转移,急需新的治疗策略提高这些患者的生存率。
KN026是康宁杰瑞自主研发的新型HER2靶向的双特异性抗体,具有良好的耐受性和安全性,在多项临床研究中显示出了对HER2阳性乳腺癌显著的抗肿瘤活性。2022年SABCS公布了KN026联合多西他赛一线治疗HER2阳性复发/转移性乳腺癌的Ⅱ期临床研究数据,客观缓解率(ORR)为76.4%,中位缓解持续时间(mDoR)为24.0个月,疾病控制率(DCR)为100%。此次临床试验申请获批,将在更多患者中继续探索KN026联合多西他赛的临床价值,希望为HER2阳性乳腺癌患者带来更有效的治疗选择。
关于KN026
KN026是康宁杰瑞采用具有自主知识产权Fc异二聚体平台技术(CRIB)开发的HER2双特异性抗体,可同时结合HER2的两个非重叠表位,导致HER2信号阻断,优于曲妥珠单抗和帕妥珠单抗联用的效果,如展示出更高的亲和力,在HER2阳性肿瘤细胞株中具备优效的肿瘤抑制作用。同时,KN026对HER2中低表达肿瘤和曲妥珠单抗抗性细胞株也有抑制作用。
KN026已于2018年分别获得中国国家药品监督管理局(NMPA)和美国食品药品监督管理局(FDA)的批准,目前正在中国、美国开展多项不同阶段临床试验,适应症包括乳腺癌、胃癌/胃食管结合部癌等,KN026联合化疗、KN026联合KN046无化疗治疗胃癌两项注册临床研究正在进行中。试验结果表明,KN026具有良好的疗效和安全性,在多线抗HER2治疗后进展的HER2阳性乳腺癌患者中仍然表现出显著的抗肿瘤活性。
2021年8月,康宁杰瑞与石药集团全资附属公司上海津曼特生物科技有限公司(以下简称“津曼特生物”)就KN026签订了在中国内地的开发及商业化授权协议。根据协议条款,津曼特生物将获得KN026在中国内地(不包括香港、澳门及台湾地区)在乳腺癌、胃癌适应症上的排他性开发与独占性商业化许可权。
文章来源:药智新闻
推荐内容: