6月28日,信达生物制药宣布,国家药品监督管理局(NMPA)已正式批准创新PD-1抑制剂达伯舒®(信迪利单抗注射液)联合达攸同®(贝伐珠单抗注射液)。
用于既往未接受过系统治疗的不可切除或转移性肝细胞癌的一线治疗。这是全球首个获批的用于肝癌患者一线治疗的PD-1免疫联合疗法。
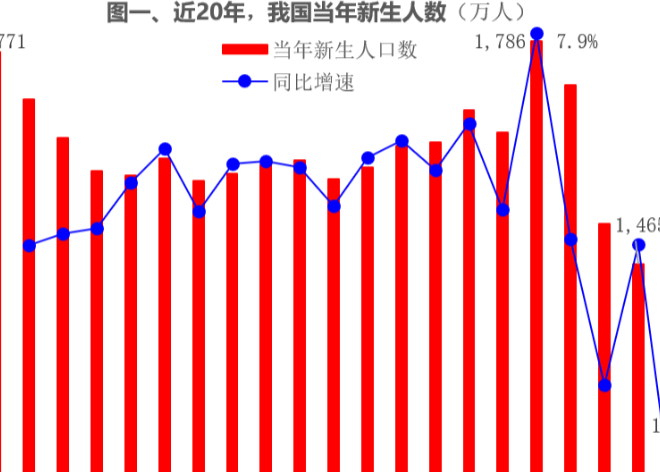
肝癌是全世界范围内常见的消化系统恶性肿瘤,中国的肝癌患者占全球数量的一半左右,肝癌严重地威胁着我国人民的生命和健康。
肝癌的病理类型主要是肝细胞癌(hepatocellular carcinoma,HCC),占85%~90%;还有少数为肝内胆管癌(intrahepatic cholangiocarcinoma,ICC)和HCC-ICC 混合型等。
在我国,HCC主要由乙型肝炎病毒(hepatitis B virus,HBV)和/或丙型肝炎病毒(hepatitis C virus,HCV)感染引起。
此次适应症获批是基于ORIENT-32研究。
该试验是一项比较达伯舒®(信迪利单抗注射液)联合达攸同®(贝伐珠单抗注射液)与索拉非尼在晚期肝癌一线治疗中的疗效和安全性的随机、对照、开放的多中心III期临床研究(ClinicalTrials.gov, NCT 03794440)。
研究共入组571例受试者,主要研究终点是总生存期(OS)和由独立影像学评审委员会(IRRC)根据RECIST v1.1标准评估的无进展生存期(PFS)。
基于独立数据监察委员会(IDMC)进行的期中分析,达伯舒®(信迪利单抗注射液)联合达攸同®(贝伐珠单抗注射液)对比索拉非尼单药治疗,显著延长了总生存期(OS)和无进展生存期(PFS)。
联合治疗方案安全性数据与既往报道一致,无新的安全性信号。ORIENT-32的研究结果全文于2021年6月15日在《柳叶刀·肿瘤学》(The Lancet Oncology)上发表。
据悉,这是达伯舒®(信迪利单抗注射液)获批的第四项适应症,也是达攸同®(贝伐珠单抗注射液)获批的第四项适应症。
2018年12月达伯舒®(信迪利单抗注射液)获得NMPA批准用于治疗复发或难治性经典型霍奇金淋巴瘤、2021年2月获得NMPA批准联合培美曲塞和铂类用于晚期非鳞状非小细胞肺癌(NSCLC)的一线治疗、2021年6月获得NMPA批准联合吉西他滨和铂类化疗用于晚期鳞状NSCLC的一线治疗。
此前达攸同®(贝伐珠单抗注射液)已获NMPA批准包括晚期非小细胞肺癌、转移性结直肠癌和成人复发性胶质母细胞瘤在内的三个适应症。
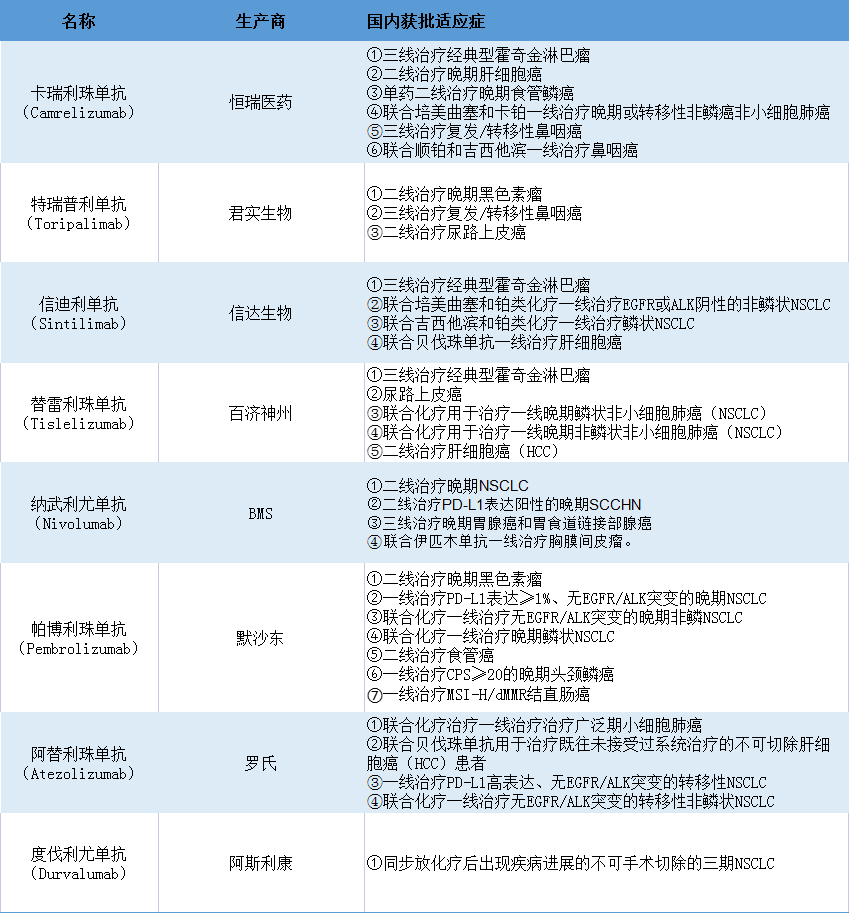
8款在中国获批的PD-1/PD-L1及适应症
推荐阅读:
283个药品不再生产了,其中就包括高血压药尼群地平,还能吃吗?
奥美沙坦是一种血管紧张素 II 受体阻滞剂,治疗高血压,耐受性良好
“神药”阿司匹林,能降低心梗、脑梗发生率,但容易发生胃肠道出血