近日李宇春在录制《我的青铜时代》时表示,自己曾因强直性脊柱炎(AS)复发一度不能睡觉,甚至需要坐轮椅出行。随后,一组李宇春坐轮椅的照片被疯传。
强直性脊柱炎(AS)是一种慢性炎性疾病,可引起脊柱、髋关节、骶髂关节等部位的损伤,导致颈、背、腰、臀部僵硬疼痛,后期严重时还可能导致关节的“融合”,使其无法活动。
据统计,AS常见于16~30岁青年人,男性多见。临床数据显示,我国AS患者已超过500万例,其中约15-100万患者有不同程度的残疾,约1/20已经引起重症残废。
AS发病原因目前尚不十分清楚,但与遗传因素和环境因素有密切的联系。目前,AS尚无法治愈,临床上主要通过手术、药物和非药物的综合治疗手段,来缓解疼痛和僵硬,或控制减轻炎症,减轻疾病进展。
AS治疗的 1.0、2.0、3.0 时代
不过随着人们对AS认知的深入,以及诊断和分类标准的不断变迁,AS治疗已经从传统药物时代进入了生物制剂时代,实现了从1.0到2.0、再到3.0时代的跨越。
1.0 时代
1.0时代,即传统治疗药物时代,治疗主要以症状控制为主。
传统的治疗药物包括非甾体抗炎药(NSAIDs)、激素、传统合成改善病情抗风湿药(csDMARDs)等,其中NSAIDs是控住症状的主要手段。
2.0 时代
2.0时代,即肿瘤坏死因子抑制剂(TNFi)时代。
TNF-α在AS中发挥重要作用,是介导AS炎症过程中核心细胞因子。大量的循证医学证据表明,相比传统药物治疗时代,TNFi可快速有效地缓解患者AS症状、降低疾病活动度。
目前已获批治疗AS的TNFi有英夫利昔单抗、阿达木单抗、戈利木单抗、依那西普、赛妥珠单抗、重组人II型肿瘤坏死因子受体-抗体融合蛋白。
3.0 时代
3.0时代,即白介素时代。
IL-17在AS发生发展的多个环节中扮演了重要角色,参与了附着点炎的发展以及病理性新骨形成过程,可导致不可逆结构损伤。
目前全球批准治疗AS的IL-17抑制剂有诺华的Cosentyx(secukinumab,司库奇尤单抗)、礼来的Taltz(ixekizumab,依奇珠单抗)、Biocad公司的Efleira(Netakimab)。
近年来AS领域还批准了几款新药,如JAK抑制剂托法替尼和乌帕替尼。这两款药物均被批准用于对一种或多种TNFi应答不充分或不耐受的活动性AS成人患者。但与上述提及的生物制剂不同,托法替尼和乌帕替尼均是小分子化药,通过口服给药。
全球在研AS新药
目前已有多款新药被开发用于治疗AS(详见下表)。可以看出在研AS新药作用靶点主要集中在IL-17和JAK,不过MK2、PDE4靶点已有相关药物被开发用于治疗AS。
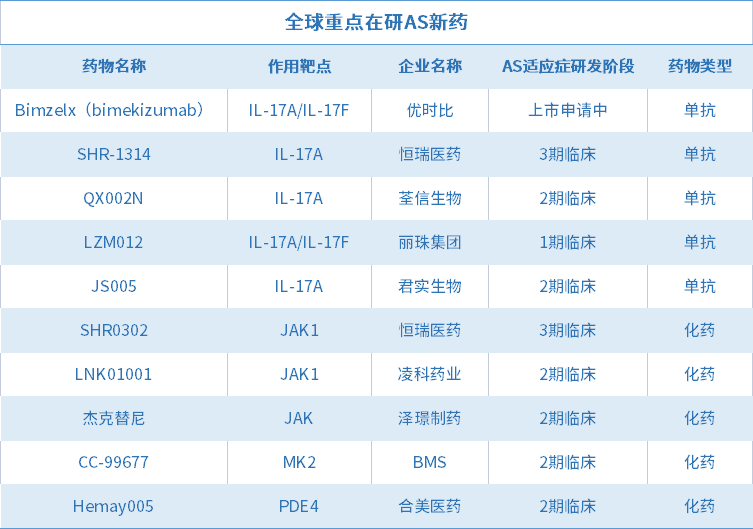
来源:公开资料
随着干细胞技术的不断进步,越来越多实验数据表明间充质干细胞是人类自身免疫性疾病细胞治疗的理想细胞选择。
研究发现,AS与自身免疫功能关系密切,AS患者血液中Th17/Treg细胞亚群的失衡导致免疫失常,免疫功能会出现明显紊乱,且出现各种组织损伤。
而脐带间充质干细胞(UC-MSCs)有较强的增殖和分化能力,移植后可在短时间内包围病灶深处的病变细胞,随着细胞在体内进一步增殖和分化,对受损细胞进行修复的同时也可以激活体内休眠的细胞,逐渐恢复其相应功能。采用MSCs移植治疗,可以纠正失衡的免疫机制,达到标本兼治的效果。
2017年《河北医学》刊发的河北衡水哈励逊国际和平医院彭肖医生及其团队的一项“间充质干细胞治疗强制性脊柱炎的临床疗效”的研究报告显示,采用间充质干细胞治疗可以有效改善AS患者的血常规和肝功能水平,患者的疼痛明显缓解,活动指数评分明显下降。
结语
由于无法根治,复发频率高,AS 又被称为“不死的癌症”。
目前,现行AS指南里的治疗药物主要是非甾体抗炎药(NSAIDs)、生物类改变病情药物(bDMARDs)、柳氮磺吡啶、糖皮质激素等。
其中,NSAIDs 常常作为一线治疗药物出现,而对NSAIDs反应不充分的患者,通常建议使用 bDMARD 治疗,但许多患者在 bDMARD 治疗中并没有达到预期的治疗目标。
而且,与 RA 或 PsA 相比,AS总体治疗选择仍然有限,仍需要更多的高效药物。
文章来源:药智新闻
推荐阅读: